सुशील जोशी
क्यों जरूरत है एटीपी की?
हमारे शरीर में तमाम किस्म की रासायनिक क्रियाएं चलती रहती हैं। हमारे ही शरीर में क्यों, समस्त जीवधरियों के शरीर में ऐसी क्रियाएं चलती रहती हैं। यदि ऊर्जा की दृष्टि से देखें तो रासायनिक क्रियाएं  दो तरह की होती हैं - ऊर्जाशोषी और ऊर्जादायक। ऊर्जाशोषी क्रियाओं को चलाने के लिए बाहर से ऊर्जा देनी होती है, जबकि ऊर्जादायक क्रियाओं के दौरान ऊर्जा निकलती है।* जब कोई क्रिया ऊर्जाशोषी है तो इसका अर्थ है कि उस क्रिया में भाग लेने वाले पदार्थों (क्रियाकारकों) की ऊर्जा, क्रिया में उत्पन्न पदार्थों (उत्पादों) की ऊर्जा से कम है। यानी इस क्रिया में ऊर्जा सोखी जाती है। इसके विपरीत ऊर्जादायक क्रिया में क्रियाकारक पदार्थों की ऊर्जा उत्पादों से ज्यादा होती है। मतलब कि इस क्रिया में ऊर्जा निकलती है। शरीर में दोनों किस्म की क्रियाएं चलती रहती हैं।
दो तरह की होती हैं - ऊर्जाशोषी और ऊर्जादायक। ऊर्जाशोषी क्रियाओं को चलाने के लिए बाहर से ऊर्जा देनी होती है, जबकि ऊर्जादायक क्रियाओं के दौरान ऊर्जा निकलती है।* जब कोई क्रिया ऊर्जाशोषी है तो इसका अर्थ है कि उस क्रिया में भाग लेने वाले पदार्थों (क्रियाकारकों) की ऊर्जा, क्रिया में उत्पन्न पदार्थों (उत्पादों) की ऊर्जा से कम है। यानी इस क्रिया में ऊर्जा सोखी जाती है। इसके विपरीत ऊर्जादायक क्रिया में क्रियाकारक पदार्थों की ऊर्जा उत्पादों से ज्यादा होती है। मतलब कि इस क्रिया में ऊर्जा निकलती है। शरीर में दोनों किस्म की क्रियाएं चलती रहती हैं।
* यहां पदार्थों की ऊर्जा, क्रिया की ऊर्जा आदि शब्दों का इस्तेमाल बहुत सटीकता से नहीं किया गया है। इन अवधारणाओं से क्या तात्पर्य है, यह शायद एक अलग लेख का विषय हो सकता है।
संक्षेप में कहें तो जीवधारियों के लिए एक समस्या यह है कि ऊर्जाशोषी क्रियाओं के लिए ऊर्जा कहां से उपलब्ध कराएं। मसलन शरीर में प्रोटीन का निर्माण करना है। सारे अमीनो अम्ल मौजूद हैं मगर यदि ऊर्जा का स्रोत नहीं है तो इनको जोड़कर प्रोटीन नहीं बनेगा। अब आपने भोजन किया उसे पचाया और मान लीजिए प्रत्येक कोशिका को ग्लूकोज प्राप्त हो गया। इस ग्लूकोज के ऑक्सीकरण से ऊर्जा प्राप्त हो सकती है। 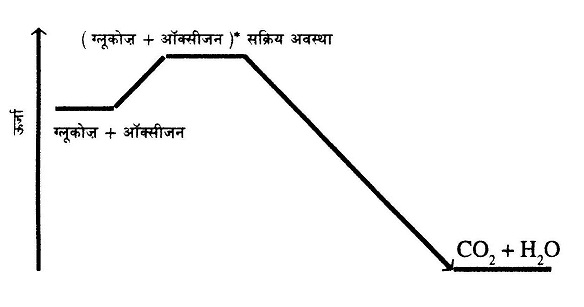 यानी इन दो क्रियाओं को (प्रोटीन का निर्माण और ग्लूकोज का आक्सीकरण) एक साथ सम्पन्न किया जाए तो ऊर्जा की समस्या हल हो सकती है। परन्तु इस व्यवस्था से एक नई जटिलता पैदा हो जाएगी। पूरे शरीर की व्यवस्था को कुछ इस ढंग से चलाना होगा कि सभी ऊर्जाशोषी व ऊर्जादायक क्रियाएं एक ही समय पर वे एक ही जगह पर चलें ताकि ऊर्जा का प्रत्यक्ष आदान-प्रदान हो सके। आप सोच ही सकते हैं कि यह व्यवस्था कितनी जटिल होगी।
यानी इन दो क्रियाओं को (प्रोटीन का निर्माण और ग्लूकोज का आक्सीकरण) एक साथ सम्पन्न किया जाए तो ऊर्जा की समस्या हल हो सकती है। परन्तु इस व्यवस्था से एक नई जटिलता पैदा हो जाएगी। पूरे शरीर की व्यवस्था को कुछ इस ढंग से चलाना होगा कि सभी ऊर्जाशोषी व ऊर्जादायक क्रियाएं एक ही समय पर वे एक ही जगह पर चलें ताकि ऊर्जा का प्रत्यक्ष आदान-प्रदान हो सके। आप सोच ही सकते हैं कि यह व्यवस्था कितनी जटिल होगी।
लेकिन अभी एक समस्या और भी है। इसे हम इस तरह समझ सकते हैं। ग्लूकोज़ का ऑक्सीकरण एक ऊर्जा दायक क्रिया है। परन्तु ग्लूकोज़ खुली हवा में, ऑक्सीजन के सम्पर्क में पड़े पड़े ऑक्सीकृत होकर ऊर्जा नहीं देता। इसका कारण यह है कि ऑक्सीजन से क्रिया करने से पूर्व ग्लूकोज़ को थोड़ी ऊर्जा की जरूरत होती है, ताकि उसका अणु इस स्थिति में आ जाए कि वह ऑक्सीजन से क्रिया कर सके। इस स्थिति को नीचे के चित्र में दर्शाया गया है।
तो समस्या यह है कि ऊर्जादायक प्रक्रिया से ऊर्जा प्राप्त करने के लिए भी शुरू में ऊर्जा देनी होती है।
लेकिन अभी एक तीसरी समस्या भी है। इसे भी ग्लूकोज़ के ही उदाहरण से ही समझते हैं। यदि आप ग्लूकोज़ को जलाएं, तो ऊर्जा प्राप्त होगी गर्मी (ऊष्मा) के रूप में। यह पानी गर्म करने के काम तो आ सकती है लेकिन इससे किसी अन्य रासायनिक अभिक्रिया को चलाया नहीं जा सकता। यानी ग्लूकोज़ का ऑक्सीकरण यदि सीधे जलाकर किया जाए तो आपको अन्य ऊर्जाशोषी क्रियाओं को चलाने के लिए ऊर्जा प्राप्त नहीं होगी।
एटीपी एक सेतु
ऊपर जिन दिक्कतों का जिक्र किया गया है उनको हल करने का सार्व भौमिक जैविक तरीका है ‘एटीपी' (एडीनोसीन ट्राइ फॉस्फेट)। दरअसल तरीका इतना ही है कि शरीर में ऊर्जादायक क्रियाओं (जैसे ग्लूकोज़ का ऑक्सीकरण) के द्वारा एक ऐसा पदार्थ बना लिया जाए जिसमें ऊर्जा संचित हो जाए। अब इस संचित ऊर्जा का उपयोग अन्य ऊर्जाशोषी क्रियाओं को चलाने के वक्त किया जा सकता है। इस प्रकार से यह पदार्थ ऊर्जादायक व ऊर्जाशोषी पदार्थों के बीच एक सेतु बन जाता है। और इस पदार्थ के कारण यह जरूरी नहीं रह जाता कि ऊर्जा दायक व ऊर्जाशोषी क्रियाएं एक साथ एक ही जगह पर चलें।
 ऊर्जादायक व ऊर्जाशोषी क्रियाओं का एक साथ, एक समय पर होना लगभग वस्तु विनिमय जैसा होगा। जबकि बीच में किसी तीसरे पदार्थ - एटीपी - का सेतु मुद्रा विनिमय की तरह है। इसीलिए एटीपी को ऊर्जा की सार्वभौमिक मुद्रा भी कहते हैं। अब सवाल यह उठता है कि इस एटीपी में क्या खास गुण है कि समस्त जीव धारियों में इसी पदार्थ को ऊर्जा-मुद्रा के रूप में इस्तेमाल किया जाता है। चलिए इसकी संरचना को देखते हैं।
ऊर्जादायक व ऊर्जाशोषी क्रियाओं का एक साथ, एक समय पर होना लगभग वस्तु विनिमय जैसा होगा। जबकि बीच में किसी तीसरे पदार्थ - एटीपी - का सेतु मुद्रा विनिमय की तरह है। इसीलिए एटीपी को ऊर्जा की सार्वभौमिक मुद्रा भी कहते हैं। अब सवाल यह उठता है कि इस एटीपी में क्या खास गुण है कि समस्त जीव धारियों में इसी पदार्थ को ऊर्जा-मुद्रा के रूप में इस्तेमाल किया जाता है। चलिए इसकी संरचना को देखते हैं।
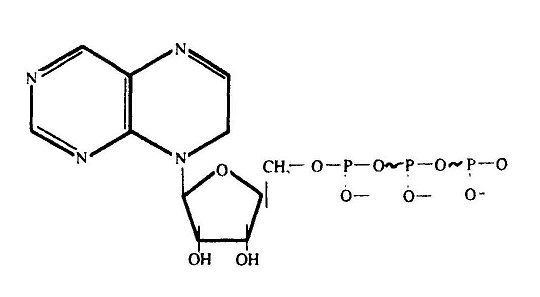
एटीपी की संरचनाः इसमें एक क्षार एडिनीन है, उससे जुड़ी राइबोज शर्करा है और उससे जुड़े तीन फॉस्फेट समूह हैं।
बढ़ते तापमान से बचना
अगर ग्लूकोज़ यूं ही जलता रहा तो निकलने वाली ऊष्मा से शरीर का तापमान इतना बढ़ जाएगा कि स्थिति जानलेवा हो जाएगी। इसलिए एटीपी के सेतु का एक महत्वपूर्ण फायदा यह है कि निकलने वाली ऊर्जा का एक बड़ा हिस्सा इसमें संचित हो जाता है।
इस अणु का जल अपघटन करने पर एक के बाद एक फॉस्फेट* समूह अलग हो जाते हैं। ऐसा होने पर ऊर्जा प्राप्त होती है। इस ऊर्जा का उपयोग विभिन्न कार्यों के लिए किया जाता है। वहीं इससे विपरीत क्रिया के दौरान यानी कि जब एडिनोसिन में फॉस्फेट समूह जुड़ते हैं तो ऊर्जा सोखी जाती है। इसीलिए ऐसा कहा जाता है कि फॉस्फेट व एडिनोसीन के बीच जो बंधन बने हैं वे उच्च ऊर्जा युक्त बंधन हैं।
दोनो क्रियाएं ही ऊर्जादायक
एटीपी के अणु में एक विशेषता और है। इस विशेषता की वजह से ही यह ऊर्जा की इतनी बेहतरीन मुद्रा है। यह तो हम जान ही चुके हैं कि एटीपी के बनने में ऊर्जा सोखी जाती है। आमतौर पर एडीपी में अकार्बनिक फॉस्फेट समूह जुड़ने से एटीपी प्राप्त होता है। इस क्रिया के लिए ऊर्जा कोई अन्य पदार्थ देता है। यह जरूरी है कि एटीपी की ऊर्जा उन सारे पदार्थों से कम हो। कहने का मतलब यह है कि एडीपी और अकार्बनिक फॉस्फेट को जोड़ने वाली क्रिया स्वयं भी ऊर्जादायक हो जाती है। दूसरी ओर जिन पदार्थों को एटीपी अपनी ऊर्जा स्थानांतरित करता है, वे भी एटीपी की तुलना में कम ऊर्जा युक्त होते हैं। इसलिए एटीपी से इन पदार्थों को ऊर्जा स्थानांतरण की क्रिया भी ऊर्जादायक हो जाती है। लिहाज़ा एटीपी का बनना तथा एटीपी से ऊर्जा का स्थानांतरण दोनों ही ऊर्जादायक क्रियाएं हैं। अतः दोनों ही क्रियाएं सहजता से हो पाती हैं। है न यह एक मजेदार तथ्य। आइए इसे थोड़ा और समझते हैं।
यह तो सही है कि एडीपी से एटीपी बनने में ऊर्जा सोखी जाती है। मगर यह क्रिया अकेली नहीं होती, बल्कि किसी-न-किसी अन्य क्रिया से जुड़कर ही होती है। जिन पदार्थों का फॉस्फेट समूह एडीपी से जुड़ता है वो हैं। फॉस्फोइनॉल पायवेट, डाई फॉस्फो गिल्सरेट तथा क्रिएटीन। जब इन पदार्थों
* आमतौर पर पहला फॉस्फेट समूह ही अलग होता है और ऊर्जा की अत्यधिक आवश्यकता के समय ही बाकी समूह इससे अलग होते हैं।
से फॉस्फेट समूह निकलकर एडीपी में जुड़ता है तो दोनों क्रियाएं मिलकर ऊर्जादायक होती हैं।
दोनों ही क्रियाएं ऊष्मादायक
एडीपी से एटीपी बनाने में प्रति मोल 7 किलो कैलोरी ऊर्जा लगती है। फॉस्फोइनॉल पायवेट, डाई फॉस्फो गिल्सरेट तथा क्रिएटीन से फॉस्फेट समूह निकलने की क्रिया में 7 किलो कैलोरी प्रति मोल से ज्यादा ऊर्जा निकलती है। इस में से 7 किलो कैलोरी प्रति मोल तो एटीपी में संचित हो जाती है और शेष ऊष्मा के रूप में प्रकट हो जाती है। अर्थात यह भी कह सकते हैं। कि उक्त पदार्थों और एडीपी से एटीपी बनाना कुल मिलाकर एक ऊष्मादायक क्रिया है। इसी प्रकार से एटीपी से जब एक फॉस्फेट समूह ग्लूकोज़ को स्थानांतरित होता है तो भी कुल मिलाकर यह एक ऊष्मादायक क्रिया होती है।
दूसरी ओर, एटीपी के जल अपघटन से एडीपी और अकार्बनिक फॉस्फेट बनता है तथा 7 किलो कैलोरी ऊर्जा प्रति मोल उत्पन्न होती है। अकार्बनिक फॉस्फेट को ग्लूकोज़ से जोड़कर ग्लूकोज़-6-फॉस्फेट बनाने में ३ किलो कैलोरी प्रति मोल ऊर्जा खर्च करना होती है।
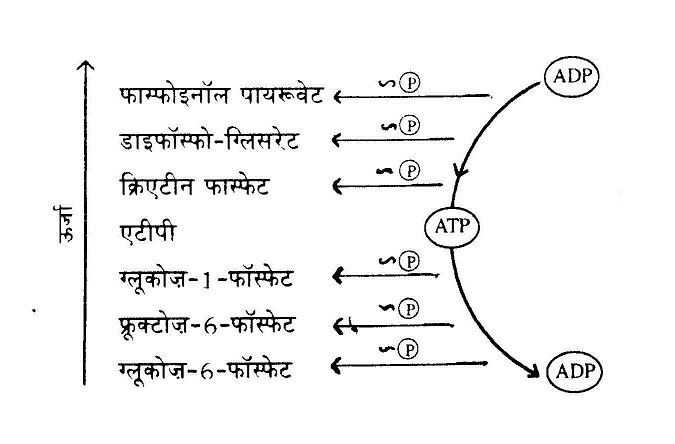 ऊर्जादायक क्रियाएं: एटीपी का बनना और एटीपी का टूटना दोनों ही ऊर्जादायक क्रियाएं हैं। रेखाचित्र का बाईं ओर का हिस्सा बताता है कि एटीपी की ऊर्जा फास्फोजन से । कम होती है और उर्जित ग्लूकोज की। ऊर्जा एटीपी से कम होती है। इसमें तीनों के लिए ऊर्जा की स्थितियां ऊपर की ओर जाते हुए तीर से दर्शाई गई हैं। दाहिनी ओर - एडीपी को फास्फोजन से एक फॉस्फेट ग्रुप मिलता है, एटीपी बनता है। इस प्रक्रिया में निकली ऊर्जा में से 7 किलो कैलोरी एटीपी में संचित हो जाती है। एटीपी का फास्फेट समूह टूटकर ग्लूकोज़ से जुड़ जाता है और ग्लूकोज़ सक्रिय अवस्था में आ जाता है।
ऊर्जादायक क्रियाएं: एटीपी का बनना और एटीपी का टूटना दोनों ही ऊर्जादायक क्रियाएं हैं। रेखाचित्र का बाईं ओर का हिस्सा बताता है कि एटीपी की ऊर्जा फास्फोजन से । कम होती है और उर्जित ग्लूकोज की। ऊर्जा एटीपी से कम होती है। इसमें तीनों के लिए ऊर्जा की स्थितियां ऊपर की ओर जाते हुए तीर से दर्शाई गई हैं। दाहिनी ओर - एडीपी को फास्फोजन से एक फॉस्फेट ग्रुप मिलता है, एटीपी बनता है। इस प्रक्रिया में निकली ऊर्जा में से 7 किलो कैलोरी एटीपी में संचित हो जाती है। एटीपी का फास्फेट समूह टूटकर ग्लूकोज़ से जुड़ जाता है और ग्लूकोज़ सक्रिय अवस्था में आ जाता है।
ATP + H2O → ADP + Pi +7 Kcal/mole
ग्लूकोज + Pi + 3 Kcal/mole → ग्लूकोज़-6-फॉस्फेट + H2O
अर्थात ATP + ग्लूकोज → ADP + ग्लूकोज-6-फॉस्फेट +4 Kcal/mole
अब यह ग्लूकोज़ अणु (ग्लूकोज़ 6-फॉस्फेट) उर्जित (Energized) अवस्था में आ गया है। यह अब आगे की क्रियाओं में भाग ले सकता है।
वास्तव में ग्लूकोज और एटीपी की यह क्रिया जीवजगत की सर्वाधिक फलदायी क्रिया है। कारण यह है कि ग्लूकोज़-6-फॉस्फेट का ऑक्सीकरण हो सकता है। इस ऑक्सीकरण के पूरा होने पर एटीपी के 36 अणुओं का निर्माण होगा। यानी एक अणु के खर्चे पर 36 अणुओं का निर्माण।
दरअसल श्वसन की पूरी क्रिया का उद्देश्य ही एटीपी का निर्माण है। जब हम कहते हैं कि श्वसन से ऊर्जा प्राप्त होती है तो तात्पर्य यही होता है कि एटीपी का उत्पादन होता है।
हमने उत्पादन की क्रिया पर अभी बिल्कुल गौर नहीं किया है। उत्पादन की इस क्रिया की दो प्रमुख बाते हैं। पहली बात तो यह है कि यह क्रिया प्रत्येक कोशिका में चलती है। एटीपी को एक कोशिका में बनाकर दूसरी कोशिका में नहीं ले जाया जा सकता। और दूसरी बात है कि एटीपी को बनाने वाली क्रियाएं अत्यंत नियंत्रित ढंग से चलती हैं। इन दोनों बातों पर चर्चा अगली बार।
मुशील जोशी: स्वतंत्र रूप से पर्यावरण और विज्ञान लेखन में सक्रिय; एकलव्य के होशंगाबाद विज्ञान शिक्षण कार्यक्रम और विज्ञान व टेक्नोलॉजी की फीचर सेवा 'स्रोत' से संबद्ध।

